Ligation-Convenience Kit
簡単・迅速ライゲーション(2 x Ligation Mix)| 品名 | Code No. | 包装単位 | 価格 | 備考 |
|---|---|---|---|---|
| Ligation-Convenience Kit | 315-05963 | 10 回用 | 3,600円 | |
| Ligation-Convenience Kit | 319-05961 | 100 回用 | 22,400円 |
製造元 (株)ニッポンジーン
表示価格は希望納入価格 (税別) です。
製品説明
Ligation-Convenience Kit はDNA ライゲーションを迅速、簡便に行うことができる2 x Ligation Mixです。本品には、DNA ライゲーションに必要な反応バッファー、ATP、DTT、T4 DNA Ligase などが全て含まれており、DNA 溶液と等量の2 x Ligation Mix を加えるだけでDNA ライゲーション反応を行うことができます。本キットを使用することで、DNA の末端形状に関わらず5 ~ 30 分間(16°C)でDNA ライゲーションを行うことができ、反応が終了したDNA 溶液はそのまま形質転換や in vitro パッケージングに使用することができます。
特長
・ 短時間(5 ~ 30 分間、16°C )で高効率なDNA ライゲーションが可能・ DNA 溶液と等量の2 x Ligation Mix を混ぜるだけ ・ DNA 末端形状の違いによる条件検討が不要・ 反応終了液をそのまま形質転換に使用可能 ・ 標準反応スケールは20 μl・ 凍結融解(50回)による反応効率の低下が無い
▲このページのトップへ
製品内容
使用回数
包装単位は20 µl反応系での使用回数です。
| 構成品 | 容量 | 保存 | 備考 |
|---|---|---|---|
| 2 x Ligation Mix |
100 μl x 1本 | -20°C |
| 構成品 | 容量 | 保存 | 備考 |
|---|---|---|---|
| 2 x Ligation Mix |
250 μl x 4本 | -20°C |
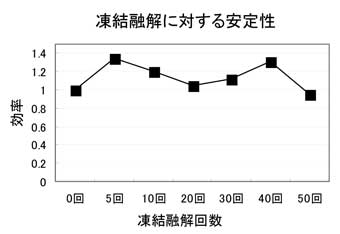
融解方法および安定性
- 使用時は氷上にて完全に融解させ、ピペッティングでよく混ぜてから使用して下さい。
- 50 回までの凍結融解による反応効率の低下は認められておりません。
▲このページのトップへ
使用例

実験例1 平滑末端ライゲーションでの性能比較
一般的にLigation効率が悪いとされる平滑末端Ligation反応での白コロニー率(Ligation効率)、コロニー数(Ligation効率および形質転換効率)について、Ligation-Convenience KitおよびA社製品、B社製品の比較を行った。
方法
- pBluescript II SK(+)をEcoRVで切断し、脱リン酸化、除タンパク後にTEバッファーに溶解した。
- λDNA由来のDNA断片500 bpをEcoRVで切断した。
- pBluescript II SK(+)50 ngとインサートDNA断片20 ng(インサート/ベクターモル比=1 : 2.4)を含むDNA溶液10 μl を調製した。
- DNA溶液10 μl に2 x Ligation Mixを10 μl 添加し、混和後、16°Cで5~60分間反応させた。反応後、JM109コンピテントセル50 μl を反応液5 μl で形質転換し、生じたコロニー数を計測した。また、比較したキットについてはそれぞれのキットのプロトコルに従って反応を行った。
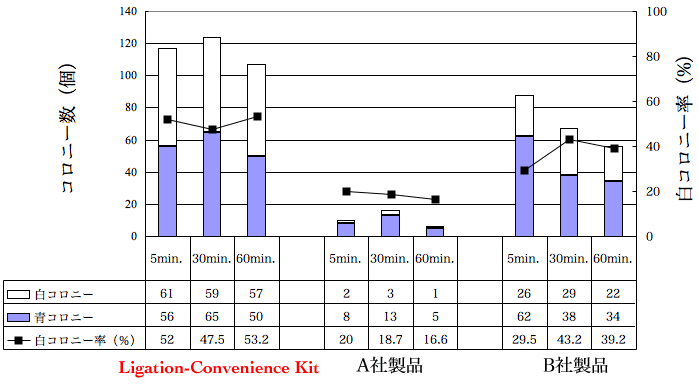
結果
Ligation-Convenience Kitでは、一般的にLigation効率が悪いとされる平滑末端でのLigation反応でも、白コロニー率(Ligation効率)、コロニー数(Ligation効率および形質転換効率)ともに良好な結果が得られた。また、反応時間は5分間で十分であった。
実験例2 ベクター:インサートモル比の検討
ライゲーションの際のベクター対インサートのモル比は、ライゲーション効率に大きく影響する。以下は、様々な長さのインサートDNA をライゲーション、形質転換した結果、それぞれの特定の条件で最もよい結果が得られたモル比である。
(1) プラスミドベクターライゲーション
| ①粘着末端 | インサート長 | 200 bp | 600 bp | 1,000 bp | 3,000 bp |
| ベクター | 1 | 1 | 1 | 1 | |
| インサート | 10 | 5〜10 | 2〜10 | 0.5〜2 |
ベクター :EcoRI で切断したpUC19(0.03 pmol)
インサート:EcoRI で切断したインサートDNA(0.015 pmol, 0.03 pmol, 0.06 pmol, 0.15 pmol, 0.3 pmol)
ライゲーション反応:16°C, 5 分間
| ②平滑末端 | インサート長 | 200 bp | 600 bp | 1,000 bp | 3,000 bp |
| ベクター | 1 | 1 | 1 | 1 | |
| インサート | 5 | 5 | 2〜10 | 0.5〜2 |
ベクター :SmaI で切断したpUC19(0.03 pmol)
インサート:SmaI で切断したインサートDNA(0.015 pmol, 0.03 pmol, 0.06 pmol, 0.15 pmol, 0.3 pmol)
ライゲーション反応:16°C, 5 分間
| ③TA クローニング |
インサート長 | 200 bp | 600 bp | 1,000 bp | 3,000 bp |
| ベクター | 1 | 1 | 1 | 1 | |
| インサート | 10 | 5 | 5 | 1 |
ベクター :pGEM® -T Easy ; Promega 社(0.03 pmol)
インサート: Gene Taq NT で増幅したPCR 産物(0.015 pmol, 0.03 pmol, 0.06 pmol, 0.15 pmol, 0.3 pmol)
ライゲーション反応:16°C, 5 分間
(2) リンカーライゲーション
| リンカー ライゲーション |
インサート長 | 8 bp |
| ベクター | 1 | |
| インサート | 50以上 |
ベクター :HincII で切断したpUC19(0.03 pmol)
インサート:Linker EcoRV (0.3 pmol,1.5 pmol, 3 pmol, 15 pmol)
ライゲーション反応:16°C, 5 分間
▲このページのトップへ
Q & A
- 1. 反応時間は本当に5分間でいいのですか?
- はい。5分間の反応時間で十分なライゲーション効率が得られます。
- 2. ライゲーションに使用するDNAはどの溶液で調製すればよいですか?
- d.dH2OやTE buffer(pH8.0)で調製して下さい。
<注意> 高塩濃度のバッファーでDNA溶液を調製すると、ライゲーション効率が著しく低下場合がありますので避けて下さい。 - 3. 凍結融解による反応効率の低下はありませんか?
- 50回の凍結融解によっても反応効率の低下は認められておりません。
- 4. 反応終了液をそのまま形質転換に使用することができますか?
- できます。
<注意> 形質転換に使用する反応液量はコンピテントセルの1/10量以下にして下さい。多量の反応液を使用した場合、形質転換効率が低下することがあります。 - 5. 反応液をそのままin vitroパッケージングに使用することはできますか?
- できます。ニッポンジーンのin vitro Packaging Kit LAMBDA INN (317-01741)やGigapack(Stratagene社)を使用した際にパッケージングを阻害しないことを確認しています。
<注意> パッケージングに用いる反応液の量はパッケージングExtractの1/10量以下にして下さい。多量の反応液を使用した場合、形質転換効率が低下することがあります。 - 6. DNA末端がどのような形状でも反応時間は5分間でいいのですか?
- はい。粘着末端、平滑末端、TAクローニング、リンカーライゲーションのいずれにおいても反応時間は5分間で十分です。
- 7. 反応時間を16時間やオーバーナイトにして使用することはできますか?
- 16時間やオーバーナイトで反応を行っても結果の大幅な改善は見られませんので、5-30分間の反応時間でご使用下さい。
<注意> オーバーナイトで反応を行うことによって形質転換効率が低下する場合があります。その場合はPCI処理を行うことで形質転換効率の低下を回避することができます。また、すぐに形質転換を行わない、または行えない場合はライゲーション反応液を-20°Cで保管して下さい。融解後はそのまま形質転換にご使用いただけます。 - 8. ライゲーションに使用するベクター量はどのくらいを目安にしたらよいですか?
- キットの標準条件である20 μlスケールにおいて約0.03pmolをお奨めします。pUC19 DNA(2,686 bp)の場合には約50 ngに相当します。使用するベクターDNAの大きさがpUC19 DNAと大幅に異なる場合も、約0.03 pmolを目安にDNA溶液を調製するとよいです。
- 9. 効率の良いライゲーションを行うにはどのようにしたらよいですか?
- ベクターとインサートのモル比を最適化することが重要です。その最適条件はDNAの末端形状、インサートの長さ、ベクターの大きさによっても異なります。ニッポンジーンではpUC19 DNA、pGEM®-T Easy(Promega社)をベクターとして使用した場合についてベクター:インサートモル比の検討を行っておりますので、ご参考下さい。
- 10. 形質転換後、残ったライゲーション反応液を保存することはできますか?
- できます。その場合は-20°Cで保管して下さい。融解後そのまま形質転換を行っても形質転換効率は低下しません。すぐに形質転換を行えない場合にもこの方法で反応液を保存しておくことで、いつでも実験を再開することができます。
- 11. 室温や25°Cでライゲーション反応を行っても問題ありませんか?
- 正確なライゲーション反応を行うためにはお奨めしません。
<注意> 反応温度を上げることで不正確なライゲーションが起こる可能性があります。例えば、不正確なライゲーションによって制限酵素サイトが潰れてしまう現象があります。この場合、コロニーPCRではインサートの導入が確認できるものの、制限酵素による再切断ができません。よって、この場合は正確なライゲーションは行われておらず、本来目的とするライゲーション産物が得られていないことになります。T4 DNA Ligaseそのものの酵素反応至適温度は37°Cであり、反応温度を37°Cに近づけることはライゲーション反応の効率が上がることを期待できますが、同時に非特異的ライゲーション等が起こる可能性も上昇し、ライゲーション反応の正確性は低下する危険性があります。 - 12. 反応スケールを下げることは可能ですか?
- 可能です。ただし、その場合は使用するDNA量も少なくして反応系全体をスケールダウンして下さい。そうすることで高効率を保持したままでのスケールダウンが可能となり、以降の実験に都合の良いスケールでご使用いただくことができます。
<注意> DNA量を減らさずに2 x Ligation Mixの使用量のみを減らした場合は、DNA量に対する試薬量が不足し、反応効率が低下する場合があります。また、極端なスケールダウンは、ピペット操作による誤差も大きくなり効率の良い条件を維持することが難しくなりますのでお奨めしません。 - 13. ライゲーション反応後に熱処理によるLigaseの失活を行うことができますか?
- 形質転換効率が著しく低下しますので反応終了液をそのまま熱処理することはできません。熱処理を行う場合は、ライゲーション反応終了液をddH2O(DNase free)で2倍希釈してから熱処理(70°C, 10分間)を行って下さい。
<注意> 熱処理後にライゲーション反応終了液を2倍希釈しても形質転換効率の低下は回避できませんのでご注意下さい。 - 14. エタチンメイト(Ethachinmate)で調製したベクターやインサートでライゲーションを行っても問題はありませんか?
- ライゲーション、形質転換ともに影響はありません。ライゲーション反応液をそのまま形質転換に使用して下さい。
<注意> エタチンメイト(Ethachinmate)の性質として、in vitroパッケージングの効率が若干下がることを確認しておりますのでご注意下さい。また、ライゲーション反応液中にエタチンメイトが存在する条件でそのままエタノール沈殿を行うと、形質転換効率が著しく低下する場合がありますのでご注意下さい。エタチンメイトを含んだライゲーション反応終了液をエタノール沈殿で濃縮する場合は、PCI処理後に行って下さい。その場合、ライゲーション反応液中に2 μl以上のエタチンメイトが持ち込まれている場合には、PCI処理後に再度エタチンメイトを添加する必要はありません。
EthachinmateとLigation-Convenience Kitを併用した場合の形質転換への影響 - 15. ライゲーション反応終了液をエタノール沈殿で濃縮する際にエタチンメイトを使用しても問題はありませんか?
- ライゲーション反応終了液をPCI処理してからエタチンメイトを添加してエタノール沈殿を行って下さい。
<注意> PCI処理を行わずにエタチンメイトを添加してエタノール沈殿を行うと、形質転換効率が著しく低下する場合がありますのでご注意下さい。また、ベクターやインサートの調製時にエタチンメイトを使用し、予め反応系にエタチンメイトが持ち込まれている場合には必ずPCI処理を行ってからエタノール沈殿を行って下さい。その場合、ライゲーション反応液中に2μl以上のエタチンメイトが持ち込まれている場合には、PCI処理後に再度エタチンメイトを添加する必要はありません。
▲このページのトップへ
資料 Data Sheet
製品マニュアル
SDS(Safety Data Sheet)
▲このページのトップへ
関連情報
備考
- 本品は試験研究用試薬です。医薬品の用途には使用しないでください。
関連製品
- ECOS Competent E. coli シリーズ
- Blunting-Convenience Kit (フラグメントの平滑化とライゲーション)
- TA-Blunt Ligation Kit (TAライゲーション、平滑末端ライゲーション専用)
- TA-Enhancer Cloning Kit (高効率TAクローニングキット)
問い合わせ先
- 購入に関するお問い合わせ先
- 富士フイルム和光純薬株式会社および同社代理店・特約店
- 富士フイルム和光純薬株式会社 製品検索サイト
- 製品に関するお問い合わせ先
- 株式会社ニッポンジーン 企画開発部
